1300万买一条命,到底值不值?
近日,中国国家药监局药品审评中心(CDE)公示,诺华(Novartis)旗下治疗脊髓性肌萎缩(Spinal Muscular Atrophy, SMA)的AAV基因治疗药物Zolgensma(OAV101注射液)在中国递交的临床试验申请已获得临床试验默示许可。
这意味这款救命药即将进入中国市场,罕见病患者多了一线生的希望。但一针高达1300万元的天价也在国内引发轩然大波。
脊髓性肌萎缩(SMA)是一种罕见的遗传性神经肌肉疾病,为渐冻症的“兄弟病症”。与“渐冻症”同样残酷,SMA患者会逐渐丧失各种运动功能,甚至无法呼吸和吞咽。只不过“渐冻症”一般是成年发病,而SMA一般是婴幼儿时期发病,同时SMA发病越早越严重。
据中国产前诊断杂志《脊髓肌肉萎缩症分子诊断与携带者筛查研究进展》的数据显示,在新生儿中,SMA发病率约为1/6000-1/10000,相当于每10000名新生儿中就有一人受此影响。2020年我国出生人口为1003万人,按万分之一发病率计算,约新增1003位患儿。
此外,SMA也是导致两岁以下婴儿死亡的首要遗传病因素,90%的患病婴儿活不过2岁。
2019年5月24日,诺华旗下的Zolgensma首先在美国获批上市。这款药物用于治疗2岁以下SMA患者,定价212.5万美元(约人民币1348万元)。患者只需接受一次静脉注射给药,就能实现长期缓解甚至治愈。加上中国,目前Zolgensma已经在全球40多个国家和地区获批。
Zolgensma的疗效在临床试验上已经获得认可,其最大的争议还是来自于定价。对于普通家庭来说,1300万元就是一个天文数字,根本无力承担。这款药物的“现实意义”几何?
一、1300万到底贵不贵?
1.首先我们站在药物研发的角度来评判这个问题
众所周知,新药研发是一项耗时费钱的任务,除了要有核心技术之外,还需要有足够的时间和资本。根据2020年发表于《美国医学会杂志》(JAMA)的一项研究显示:一个新药的中位研发成本约10亿美元,平均成本为13亿美元!肿瘤和免疫调节药物的研发成本更高,平均数为45亿美元。
(来源:《美国医学会杂志》 )
另外,在研发时间上,则需要10到15年,主要经历化合物研究、临床前研究、临床试验、上市四个关键阶段。其中,第三阶段“临床试验”最为耗时,一般需要6到7年。
这还是站在药物研发成功的基础上,如果失败了,一切都将付诸东流。根据数据统计,全球范围内,新药研发临床I、II、III期的平均成功率分别为63.2%、30.7%和58.1%,按照这个比例计算,从I期到上市,新药临床研究的成功率不到10%。
普通新药尚且如此,不受人待见的“罕见药”在研发上只会更加艰难。
《我不是药神》中的白血病神药“格列卫”同样由诺华研制,但整整花了41年、总投入14亿美元才得以研发成功。
虽然Zolgensma并非由诺华亲手研发,而是通过87亿美元收购AveXis公司获得,成本也颇高。并且在研发周期上,这款药物自2013年便开始了临床试验。
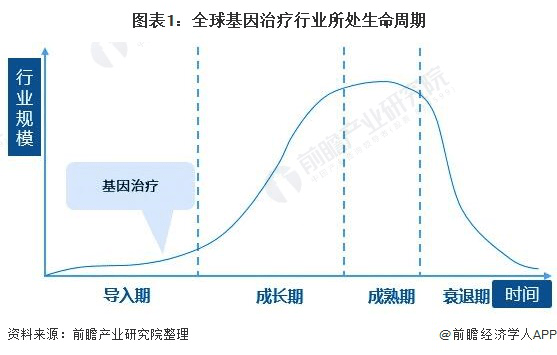
在技术方面,Zolgensma采取的是一种新型治疗方式——基因疗法。基因疗法虽被称为最具前景的生命医疗发展方向,但目前还处于发展早期。前瞻产业研究院发布的报告显示:整体来看,全球基因治疗行业仍处于导入期。基因治疗的技术研发到产品应用仍有较长路要走。
2.企业掌握“罕见药”自主定价
“罕见药”价格不仅受研发成本的影响,定价策略也同样重要。
统计显示,罕见药定价一般为非罕见药的6-7倍。就罕见药来说,企业一般均有自主定价权,由于罕见药市场需求相对较小,唯有较高的定价才能取得足够的投资回报。而美国罕见药法案又给予罕见药企业很大的自主定价权,全球最贵的药物中,几乎都是罕见药。
目前罕见药定价原理和方法主要包括“成本加成法(Cost plus pricing,CPP)”和“以价值为基础的定价方法(Value-based pricing,VBP)”。后者在很多发达国家已成为创新药物定价的金标准,但目前罕见药的补偿价格还是以成本加成定价方法为主。
(来源:医药经济报)
但无论是CPP还是VBP,其中最关键的变量是研发成本和患者人数。
“罕见药”研发成本高企是不争的事实,然而潜在用药患者人数又极其有限,何况Zolgensma还只针对I型SMA,患者更加少。成本分摊到每个人的头上,自然就造成了定价居高不下。
根据诺华官网,自2019年上市至现在,全球共1600名儿童使用Zolgensma,按照212万美元的定价,可收回约34亿美元。但在付款方面,诺华提供最长5年分期。因此34亿美元中有相当一部分款项可能并未到位,这可从诺华公布的财报中得到佐证。
据诺华的财报,2020年Zolgensma的销售额达9.2亿美元。2021年前三季度Zolgensma销售额合计10.09亿美元。预计过去两年销售额合计约23亿美元。
这个数字距离诺华在Zolgensma上投入的成本还有很大的差距。未来,Zolgensma能否收回成本并实现盈利还是个未知数。
而面对社会和舆论的质疑,诺华公司CEO曾表示:“那些批评者并没有真正思考我们的医疗系统怎么运作的。我们给病人做移植手术,每个病人要花300万到500万美元,但是效果远不如这些药物。如果这种疗法只进行一次,费用比目前的疗法都要便宜。”
二、“天价药”能否纳入医保变“救命良药”?
实际上,Zolgensma并非首个震惊市场的同类“天价药”。
在Zolgensma问世以前,于2016年年底获美国FDA加速批准的渤健Spinraza(诺西那生钠注射液)是治疗SMA的全球首款药物。该药的总费用远高于Zolgensma。
与Zolgensma只需注射一次不同,Spinraza需要长期用药,治疗第一年花费75万美元,此后每年37.5万美元,治疗10年的费用高达410万美元(约人民币2600万元)。2019年,Spinraza被批准中国上市,定价接近70万一针,第一年打6针,之后每4个月就要打1针。
Spinraza刚在中国上市的时候给患儿带来了生的希望。然而,仅第一年就需自费420万,普通家庭根本无力承受。
幸运的是,2021年12月迎来了振奋人心的消息——70万一针的药物被纳入医保,降价至3万多。除第一年外,每年药费从210万降至10万。
有鉴于此,民众也纷纷期待Zolgensma被纳入医保。但希望很可能落空!
据北京病痛挑战公益基金会统计,2021年国家医保目录谈判后,有28种罕见病的58种药物已经纳入国家医保目录。虽然被纳入医保的罕见病药物无论是从量上、还是从高价上较以往都有所突破,但有一点需要注意:医保不能为所有高值药物托底也是业界共识!
国家医保谈判药品基金测算专家组组长郑杰曾公开表示,“目前国家医保目录内所有药品年治疗费用均未超过30万元”,并称,未来国家医保局将“坚决杜绝天价药进医保”。承担着“保基本”这一功能定位的国家医保目录,决定了能够被纳入其中的药品必须具备“价格合理”这一基本条件。
而与Zolgensma相比,同为治疗SMA的Spinraza之所以能被纳入医保主要有三点原因:
1.Spinraza不是新药,它在全球市场已经基本盈利;
2.中国SMA儿童人数较多,药物市场很大。并且与Zolgensma只针对I型SMA相比,Spinraza可治疗不同类型的SMA。
3.Spinraza的厂商渤健在战略选择了投了中国一票。
三、做好婚检和产检,是避免SMA最有效的方法
与其苦恼让“天价药”变成“救命良药”,不如从源头上就遏止病魔。做好婚检和产检是避免花费1300万一针的最有效办法,还可以挽救无数的家庭。
从发病机制来看,SMA是由于人体内称作为SMN1基因突变或异常所导致的。对于健全人而言,这一基因可以制造出一种被称为SMN的蛋白。若此基因异常的话,人体内的SMN蛋白就会缺失或显著减少,进而导致运动神经元出现严重的问题。
患儿父母通常各自只有一个SMN1基因有缺陷,所以并不会得SMA,也不会表现出患病的症状,他们被称作为携带者。当父母各自把这个缺陷基因遗传给孩子时,才会导致孩子获得了两个有缺陷的基因拷贝而染病。
常规人群,约每50人中就有1个是SMA致病基因的携带者,父母同为携带者,他们每次怀孕就有:
① 25%的几率孩子会是SMA患者;
② 50%的几率孩子会是SMA致病基因携带者;
③ 25%的几率孩子会是健康的。
SMA婴儿就像一个家族报警器,经常是孩子生出来了,才会倒推出父母是携带者,为什么不能提早发现呢?在这种情况下,通过婚检和孕检筛查出SMA携带者就显得尤其重要。
对SMA等遗传性疾病,通过携带者筛查提前预防疾病的发生是更为有效的解决方案。所谓携带者筛查,是指通过基因检测的方式在群体中将表型正常的常染色体隐性遗传病携带者筛出,并对其进行风险评估和婚育指导,避免生出SMA患儿。
然而,我国婚检率目前仍不太理想。数据显示:目前全国的婚检率仅62.4%,离100%的目标还有较长距离。一些发达城市甚至未达平均线,例如北京婚检率仅为54.08%。此外,虽然我国推行免费婚检,婚检项目中也包括先天性遗传疾病筛查,但覆盖范围较小,很多罕见病未被纳入。在婚检率尙不高的情况下,更不用说有多少准夫妇会自费筛查SMA等致病基因。
为了进一步降低新生儿出生缺陷率,国家正在大力提高民众婚检意识,并在婚检项目中加大关于基因筛查的项目。
如果在婚检中遗漏了相关基因筛查,还有一个补救方法——产前做好SMA基因检测。
从婚检到产检,形成SMA筛查的闭环,真正预防出生缺陷,让新生儿迎来“新生”,让每一个家庭真正沉浸在“新生”的喜悦中。在当下,这可能更具有现实意义。
关键词: 临床试验 申请 已获得 Zolgensma
 首页
首页












 营业执照公示信息
营业执照公示信息